Загадки хронической усталости при болезни Паркинсона
В.К.Датиева, О.СЛевин[1]
Более чем у половины пациентов с болезнью Паркинсона (БП) выявляется особое состояние, которое в настоящее время принято обозначать как синдром хронической усталости (СХУ). Под ним понимают состояние крайнего утомления, слабости, истощения, упадка сил (физических и/или психических), наступающее в результате выполнения привычной для больного нагрузки и ограничивающее его функциональную активность. СХУ является одним из основных факторов, влияющих на качество жизни пациентов. Между тем, механизмы его развития, вопросы диагностики и лечения пока недостаточно разработаны [1-4,8].
Больные с СХУ нередко жалуются на дефицит энергии, выносливости, мотивации. С патогенетической точки зрения выделяют первичную и вторичную усталость. При первичной усталости рассматриваемый феномен является самостоятельным синдромом. Вторичная усталость обусловлена депрессией, вегетативной недостаточностью, нарушением сна и бодрствования и другими расстройствами. Тем не менее многие предполагают, что невозможно разграничить первичный и вторичный (вызванный сопутствующими нарушениями) СХУ [11, 13].
Выделяют также периферический и центральный типы усталости. Периферический тип сопровождается мышечной (физической) усталостью. Центральная усталость при БП имеет как психические, так и физические аспекты и сопровождается снижением порога утомляемости [8, 15, 28, 30, 34].
Диагностика синдрома хронической усталости
На сегодняшний день не существует идеального инструмента для диагностики и оценки СХУ [17, 25]. Наиболее часто для диагностики и количественной оценки СХУ у пациентов с БП применяются следующие шкалы (опросники).
Шкала тяжести усталости (Fatigue Severity Scale):
Моя мотивация снижается, когда я устаю.
Физическая нагрузка влияет на мою утомляемость.
Я очень быстро устаю.
Усталость нарушает мою повседневную деятельность.
Усталость часто создает различные проблемы для меня.
Усталость даже предшествует физической нагрузке.
Усталость мешает мне выполнять мои обязанности.
Усталость — один из трех основных симптомов, мешающих мне.
Усталость создает для меня проблемы в работе, семейной жизни и социальной сфере.
Каждое утверждение пациент должен оценить, поставив балл от 1 до 7: 1 балл — совершенно не согласен; 7 баллов — совершенно согласен. Баллы по каждому пункту суммируются и делятся на 9. Если полученный результат будет >4, усталость считается клинически выраженной.
Шкала усталости при БП (Parkinson’s Fatigue Scale):
В течение дня мне необходим отдых.
Я вынужден изменить свой образ жизни из-за усталости.
Я знаю, что устаю быстрее, чем другие люди.
Усталость — один из трех самых неприятных для меня симптомов.
Я чувствую себя «выжатым, как лимон».
Усталость мешает мне активно проявлять себя в социальной жизни.
Мне требуется больше времени для выполнения заданий из-за усталости.
Я испытываю чувство тяжести.
Если бы я так не уставал, я больше успевал бы в течение дня.
Все, что я делаю, я делаю с усилием.
Мне не хватает энергии большую часть времени.
Я чувствую себя полностью опустошенным.
Усталость препятствует моей привычной деятельности. Я чувствую себя уставшим, даже когда еще ничего не успел сделать.
Из-за усталости я делаю меньше, чем мне хотелось бы.
Я бываю таким уставшим, что мне хочется лечь, где бы я ни находился.
Каждое утверждение пациент должен оценить от 1 до 5 баллов: 1 балл — совершенно не согласен; 5 — совершенно согласен. При среднем балле >3,3 усталость считается клинически значимой.
Связь синдрома хронической усталости с другими проявлениями болезни Паркинсона
СХУ часто сопутствует другим немоторным проявлениям БП. Более высокое число сопутствующих симптомов ассоциируется с более тяжелым двигательным дефицитом при БП [18, 19]. СХУ нередко связан с депрессией, тревогой, апатией, болью, нарушением сна и бодрствования, диз- регуляторным когнитивным синдромом. Частое выявление этих симптомов уже на ранней стадии БП, последующее их развитие или утяжеление в периоде «выключения» у пациентов с флуктуациями, нередкое их появление после оперативного вмешательства на фоне резкого снижения дозы дофаминергических средств говорят о гиподофаминерги- ческой природе указанных расстройств [7]. Безусловно, каждое из этих проявлений имеет сложный гетерогенный характер и может быть связано с разными механизмами, тем не менее их сочетание может указывать на необходимость усиления дофаминергической терапии [6, 8,11].
Большинство сравнительных исследований не выявило связи между СХУ и тяжестью двигательных симптомов БП, оцениваемых по шкале Хен-Яра, а также шкале UPDRS.
Синдром хронической усталости и нарушения сна
Нарушение цикла «сон-бодрствование», сопровождающееся расстройством ночного сна и повышенной дневной сонливостью (ПДС), часто сочетается с СХУ Клинически значимое нарушение сна и бодрствования отмечается у 60-90% пациентов с БП [18, 19]. Утрата нейронов, синтезирующих орексин и мелатонин, является одной из возможных причин диссомнических расстройств при БП.
Нарушения сна могут проявляться уже в продромальной стадии, а могут впервые возникнуть лишь в поздней
Рис. 1. Взаимозависимый цикл симптомов при БП.
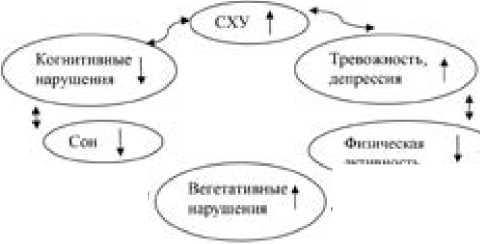
Некоторые исследования предполагают самостоятельный характер феномена хронической усталости при БП, не усматривая причинной связи с дневной сонливостью или расстройством ночного сна [41]. Как и сонливость, СХУ не зависит от моторных проявлений заболевания, их изменений на фоне терапии.
Синдром обструктивных апноэ во сне нередко вызывает развитие как синдрома усталости, так и дневную сонливость. У мужчин повышенного питания, жалующихся на сильный ночной храп, которым требуется частый дневной сон, целесообразно проведение скрининга апноэ во сне. Коррекция синдрома обструктивных апноэ, лежащего в основе синдрома усталости, приводит к значительному улучшению состояния пациента.
Особое внимание в последнее время уделяется проблеме ПДС и «атакам сонливости», определяемым как эпизоды короткого непреодолимого сна в несоответствующей обстановке, в том числе за рулем автомобиля, а также их связи с использованием дофаминергических препаратов. Сонливость, вероятно, является одной из составляющих БП, отражает выраженность нейродегене- ративного процесса. Некоторые авторы рассматривают расстройства бодрствования как результат нарушений ночного сна, часто встречающихся при БП (апноэ во сне, инсомнии с фрагментацией структуры сна, укорочением фазы быстрого и стадии 3 фазы медленного сна) [32]. Однако исследования сна у больных БП с использованием полисомнографии продемонстрировали возможность существования дневной сонливости как одного из начальных симптомов БП, не связанного с лечением и нарушениями ночного сна. G.Alves и соавт. обнаружили корреляцию между СХУ и ПДС при БП [15]. В то же время пациенты с СХУ остаются уставшими даже после дневного сна, тогда как большинство людей с неудовлетворительным ночным сном после дневного отдыха чувствуют облегчение.
стадии БП. В структуре расстройств сна следует различать первичные нарушения, формирующиеся в отсутствие противопаркинсонической терапии, и вторичные, обусловленные противопаркинсонической терапией. Причиной расстройства сна могут быть также нарастание в ночное время двигательных нарушений, в том числе дистонии периода «выключения», тремора, гипокинезии, ригидности, трудности при изменении положения тела во время сна. У пациентов с БП в развернутой и поздней стадии заболевания нередко наблюдаются «ночные» ней- ропсихиатрические симптомы в виде ярких сновидений, ночных кошмаров, ночных галлюцинаций.
Изменение суточного ритма у лиц с синдромом хронической усталости
Подавляющее большинство пациентов с БП отмечают колебание симптомов заболевания в течение дня [5]. После сна некоторые больные чувствуют себя лучше на протяжении нескольких десятков минут и даже часов. Ухудшение состояния часто развивается к обеду и к вечеру. Нарушение сна и бодрствования при БП является одним из проявлений расстройств циркадного ритма. Эффект противопаркинсонических препаратов в течение дня также неравномерен. На фоне длительного приема препаратов леводопы в связи с развитием флуктуаций появляется соответствующая ритмика как моторных, так и немоторных симптомов. Нарушение суточного ритма проявляется и многочисленными вегетативными расстройствами при БП: утратой закономерных колебаний артериального давления (АД) в течение суток (например, отсутствием ночного снижения АД), а с другой стороны, нестабильностью АД в течение дня (например, пост- прандиальной гипотензией — быстрым снижением АД после приема пищи). Наши исследования показывают, что у лиц с СХУ чаще отмечается нарушение суточной ритмики, а ее коррекция (например, с помощью препаратов мелатонина) сопровождается снижением усталости. Однако данная закономерность требует дальнейшего исследования.
Нейромедиаторные изменения при синдроме хронической усталости
Предполагается, что СХУ может быть следствием нейрональной дегенерации в зонах мозга, ответственных за мотивационно обусловленное поведение. К таким мозговым «центрам вознаграждения», поддерживающим мотивацию, относят дофаминергические проекции, связывающие вентральную покрышку ствола мозга с лимбической системой [10, 31, 32].
Выраженность двигательных нарушений обычно коррелирует с численностью транспортеров дофамина, определяемых с помощью однофотонной эмиссионной компьютерной томографии (ОФЭКТ) с В11-йодбензамидом, однако зависимости СХУ от нейровизуализационных показателей, отражающих денервацию скорлупы, обнаружено не было.
N.Pavese и соавт. в 2010 г. изучали зависимость усталости от дофаминергической и серотонинергической дисфункции на уровне базальных ганглиев и лимбических структур. Результаты исследования продемонстрировали у пациентов с СХУ уменьшение накопления радиолиганда 18F-DOPA с обеих сторон в области хвостатых ядер, скорлупы, а также в островке. Кроме того, N.Pavese и соавт. обнаружили у тех же пациентов билатеральное уменьшение »С-ЛАБВ-стимулированной активации хвостатого ядра, скорлупы, вентрального стриатума, таламуса, поясной извилины, миндалины. Авторы пришли к выводу, что СХУ при БП главным образом ассоциируется с серотонинергической денервацией дорсального и вентрального стриатума, таламуса, а также экстрастриарной дофаминергической дисфункцией [36]. Дисфункция норадренергической системы также может играть важную роль в развитии СХУ [7, 14, 19].
Когнитивные расстройства и синдром хронической усталости
В небольшом исследовании была выявлена связь между тяжестью проявлений СХУ, депрессией, дизрегулятор- ным синдромом и снижением перфузии лобных долей [9]. По другим данным, СХУ ассоциируется с замедлением скорости ходьбы во время упражнений, требующих повышенного внимания [33]. Авторы предположили, что умственное напряжение при осуществлении когнитивных процессов способствует развитию СХУ и дистрессу, а не наоборот.
В норвежском исследовании, изучившем развитие СХУ при БП в течение 8 лет, была обнаружена корреляция между снижением баллов по шкале MMSE и нарастанием жалоб на усталость. Наиболее выражены психические компоненты усталости, что обычно сопровождается ухудшением внимания, сниженной мотивацией, аффективными нарушениями. Следует отметить, что и когнитивные нарушения, и СХУ не зависят от тяжести двигательных симптомов при БП. Коррекция когнитивных расстройств (например, мемантином) оказывает некоторое положительное влияние на феномен хронической усталости [9].
Синдром хронической усталости и физическая активность
Пациентам с БП свойственна повышенная мышечная утомляемость в сравнении со здоровой популяцией. Показано, что на фоне физической активности проявления СХУ возникают на 50% быстрее, чем в контрольной группе (при отсутствии различий в максимальной силе сокращения мышц). Некоторые специалисты отметили повышенную усталость у больных БП во время выполнения пробы на гипокинезию, которая уменьшалась после приема леводопы. Covington и соавт. описывают положительную обратную связь между болью, депрессией, СХУ, снижением двигательной активности [34].
Интерес вызывает сообщение X.Chen и соавт. о снижении качества физической деятельности у пациентов с БП: за 12 лет до установления диагноза у мужчин и за 2-4 года — у женщин [21]. Оценка СХУ в этом исследовании не проводилась, поэтому остается неясным влияние данного феномена на состояние физической активности.
Кроме того, обнаружено, что больным БП отдых не приносит такого чувства облегчения, как здоровым лицам. Во время выполнения физических упражнений энергетические затраты на работу дыхательной мускулатуры у пациентов с БП больше. Однако различий между эффективностью расходования энергии во время работы у больных БП, сочетающейся с СХУ или протекающей без СХУ, не было [34].
Для определения физиологических механизмов СХУ J.S.Lou и соавт. оценивали возбудимость двигательных нейронов коры во время и после упражнений с нагрузкой на лучевой разгибатель кисти. У больных БП было зарегистрировано увеличение амплитуды вызванного двигательного потенциала, а также более выраженное посленагрузочное расслабление в сравнении с пациентами контрольной группы. Указанные изменения исчезали после назначения препаратов леводопы. Результаты дан
ного исследования позволяют предположить, что СХУ при БП обусловлен прежде всего измененной возбудимостью двигательных нейронов коры, а не утомлением мышечных волокон.
Синдром хронической усталости и вегетативная недостаточность
Некоторые исследования указывают на возможное участие вегетативных нарушений, прежде всего ортостатической гипотензии (ОГ), в патогенезе СХУ ОГ развивается у 20-65% пациентов с БП [37]. ОГ может проявляться генерализованной слабостью, головокружением, в тяжелых случаях — эпизодами потери сознания. ОГ увеличивает риск падений и когнитивных нарушений. У пожилых пациентов ОГ является фактором риска повышенной смертности. ОГ может проявляться до дебюта двигательных нарушений, позволяющих диагностировать БП. ОГ может быть вызвана, с одной стороны, симпатической денервацией сердца, с другой, нарушением вазоконстрикции из-за симпатической денервации сосудов (согласно гипотезе «двойного удара»). Симпатическую денервацию сердца может подтвердить ОФЭКТ с радиолигандом 12,1-метайодобензилгуанидином. Появление симптомов усталости может быть связано с уменьшением силы сердечного сокращения во время физических упражнений [35]. Область поражения в центральной нервной системе, вызывающая нарушение барорефлекса при БП, лежащее в основе ОГ, не идентифицирована [27]. Предположительно, ОГ бывает вызвана гибелью клеток и накоплением телец Леви в области голубоватого пятна — главного источника норадреналина в головном мозге. Провоцировать развитие или усиливать проявления ОГ могут некоторые лекарственные препараты. Назначение леводопы или агонистов дофаминовых рецепторов (АДР) может вызвать или усугубить ОГ. Другими препаратами, способными провоцировать развитие ОГ, являются антигипертензивные средства, диуретики, антидепрессанты, нейролептики.
Влияние дофаминергической терапии на синдром хронической усталости
В исследовании ELLDOPA было также показано, что у больных, принимавших в течение 42 нед. плацебо, проявления СХУ усугубились по сравнению с пациентами, которые в течение этого срока получали леводопу. Однако данная связь не носила дозозависимый характер. Интерес вызывает факт наибольшей эффективности препаратов леводопы в группе наблюдения, в которой исходно отсутствовал СХУ
Исследование P.O.Valko и соавт. выявило более значительное влияние дофаминергической терапии на ИДС, чем СХУ Была обнаружена слабая, но, тем не менее, значимая связь между эквивалентной дозой леводопы и оценкой по шкале сонливости по Epworth (ESS) [40]. P.O.Valko и соавт. обнаружили также, что у пациентов с БП СХУ не связан ни с частыми ночными пробуждениями, ни с периодическими движениями конечностями во сне, что также согласуется с гипотезой о центральном происхождении СХУ [40]. Такой же результат получила и канадская группа исследователей (Canadian Movement Disorder group) на примере 638 пациентов с БП при использовании разных режимов дофаминергической терапии. Сравнивая больных, находящихся на монотерапии леводопой, с пациентами, получающими леводопу и АДР, а именно прамипексол или ропинирол, исследователи получили значимые различия по шкале ESS, но не по FSS [40]. Paus и соавт. отметили более высокий риск внезапных приступов непреодолимой сонливости у больных, получающих комбинированную терапию леводопой и АДР, в сравнении с монотерапией леводопой. Fabbrini и соавт. не обнаружили корреляции между суммарным баллом, полученным при оценке сна по Питтсбургскому опроснику (Pittsburgh sleep questionnaire), и оценкой по шкале ESS у пациентов с БП. Это говорит о том, что ПДС обусловлена не первичным расстройством ночного сна, а, скорее, непосредственно нейроде- генеративным процессом.
Синдром хронической усталости и воспаление
В целом ряде исследований показано, что нейродегене- ративный процесс, в том числе при БП, сопровождается неспецифическим нейрогенным воспалением. Носят ли указанные процессы нейропротективный или нейротоксический характер, еще предстоит выяснить [12]. При гистологическом исследовании материала, взятого из головного мозга пациентов с БП, было обнаружено повышенное содержание провоспалительных агентов: циклооксигеназы-2, провоспалительных цитокинов, в том числе интерлейкина-ip, фактора некроза опухолей а, интерферона-у. С подобными данными согласуется недавно завершившееся исследование по протективному действию ингибиторов митоген-активируемой протеин- киназы, которые оказывают защитное действие на нейроны черной субстанции, тормозя активность тромбина и протромбина. При этом микроглия остается в состоянии покоя. Эти результаты подтверждают повреждающее действие окислительного стресса на микроглию и влияние провоспалительных агентов на дофаминергические нейроны черной субстанции. Помимо микроглии в патогенезе БП предполагается участие астроцитов, различных нейротрофических факторов (таких как глиальный нейротрофический фактор, мозговой нейротрофический фактор, ресничный нейротрофический фактор). Астроциты играют защитную роль, способствуя поддержанию функциональной активности дофаминергических нейронов. Кроме того, именно они осуществляют синтез различных нейротрофических факторов, упоминавшихся ранее. Известно, что астроциты играют важную роль в антиоксидантной системе головного мозга.
Подобные факты делают привлекательными попытки воздействия на процесс нейрогенного воспаления. Был установлен протективный эффект фемтомолярных концентраций дексаметазона на мезэнцефальные дофаминергические нейроны путем уменьшения содержания супероксидов и провоспалительных цитокинов. В недавнем исследовании схожий протективный эффект, связанный с редукцией глиальной активации, сопровождающейся каскадом воспалительных процессов, был продемонстрирован у симвастатина [26]. Флуоксетин, известный антидепрессант, проявил антиоксидантное
свойство и нейропротективный эффект. X.Chen и соавт. в исследованиях на экспериментальной модели паркинсонизма. полученной с помощью 1-метил-4-фенил-1,2,3,6- тетрагидропиридина (МРТР), обнаружили, что кофеин уменьшает гибель дофаминергических нейронов [21]. Индометацин оказывает нейропротекторное действие на дофаминергические нейроны, уменьшая количество активных иммунных клеток в области черной субстанции у экспериментальных животных, подвергнутых действию МРТР. Существуют данные о схожем эффекте синтетического каннабиоида WIN55,212-2, уменьшающего не только микроглиальную активацию, но и процессы перекисного окисления, проницаемость гематоэнцефалического барьера, инфильтрацию ЦНС иммунными клетками.
Коррекция синдрома хронической усталости
Высокая распространенность и клиническое значение СХУ делают необходимой разработку подходов к терапии данного синдрома [29, 33].
Быстрых и эффективных способов лечения СХУ не существует, поскольку до сих пор неизвестна его основная причина или комплекс причин. Терапия имеет преимущественно симптоматический характер. Помимо медикаментозной терапии чрезвычайно важной является модификация образа жизни с включением в него дозированных физических упражнений. Чрезмерная физическая нагрузка может усугубить этот синдром. Важное значение имеет адекватная коррекция противопаркинсо- нической терапии и лечение коморбидных расстройств, прежде всего депрессии, нарушений сна, повышенной сонливости, ортостатической гипотензии. Лечение сопутствующих СХУ депрессии или дневной сонливости оказывает положительное влияние на коррекцию самого СХУ [16]. Однако для коррекции СХУ, проявляющегося у пациентов в отсутствие указанных нарушений, эффективного средства пока не найдено.
Для фармакологического лечения усталости в разные годы использовали более 40 различных препаратов: психотропные средства, преимущественно антидепрессанты и психостимуляторы, общеукрепляющие средства, адап- тогены, витамины, препараты, улучшающие метаболизм головного мозга, и др. [1, 2, 4]. Более или менее гарантированный эффект оказывают психостимуляторы, однако их антиастеническое действие после окончания терапии часто бывает нестойким и сходит на нет в течение нескольких дней или недель, а иногда «ускользает» на фоне их продолжающегося приема [3]. Применение плацебо может быть полезным у части больных.
G.Schifitto и соавт. (2008) продемонстрировали, что СХУ у пациентов, которые после установления диагноза БП принимали препараты леводопы, нарастал в меньшей степени, чем у больных, получавших плацебо [38]. Амантадин, используемый для коррекции синдрома усталости при рассеянном склерозе, оказался недостаточно эффективным в лечении СХУ при БП. Селегилин также не оказывает влияния на СХУ при БП. Однако разагилин в дозе 1 мг/сут. уменьшает проявления хронической усталости.
Модафинил (психостимулятор, широко используемый в западных странах для коррекции ПДС) в дозе 400 мг/сут. при длительном применении (5 мес.) не проявил положительного эффекта в отношении СХУ Постмаркетинговые исследования модафинила показали возможность развития в редких случаях (1-2 случая на 1000000 человек в год) тяжелого дерматита, в том числе токсического эпидермального некролиза, синдрома Стивенса-Джонсона, лекарственной сыпи с эозинофилией и системными проявлениями. Психиатрические осложнения (мания, бред, галлюцинации, суицидальные мысли, агрессия) развивались у пациентов, получающих модафинил, у которых в анамнезе уже отмечались подобные нарушения. Данных, касающихся влияния модафинила на сердечно-сосудистую систему, в частности повышения АД и появления тахикардии при его назначении, недостаточно для однозначного решения о профиле безопасности этого препарата.
Работа Ondo и соавт. (2008) продемонстрировала эффективность лечения СХУ оксибатом натрия. По мнению М.Р.Нодель [13], выявленное положительное влияние прамипексола на повышенную утомляемость может быть связано с действием этого препарата на D,-рецепторы мезолимбической дофаминергической системы. В то же время неоднократно отмечено усиление хронической усталости на фоне длительного приема АДР.
K.L.Chou и соавт. (2012) изучали влияние стимуляции глубинных структур головного мозга, в частности субталамического ядра, на клинические проявления СХУ На примере 17 пациентов они не выявили улучшения при оценке по шкале PFS спустя 6 мес. после такого вмешательства. Однако 6 из 17 пациентов отметили уменьшение проявлений СХУ, у 3 больных эти проявления усилились, 8 пациентов не отметили никаких изменений. Авторы исследования предполагают, что, несмотря на малое число наблюдений, можно говорить о влиянии стимуляции глубинных структур головного мозга на СХУ, хотя ответ пациентов с этим синдромом на такое лечение был крайне вариабельным. Полагают, что улучшение показателей СХУ после оперативного вмешательства связано с улучшением двигательных функций и настроения.
Этилтиобензимидазол, или Метапрот (аббревиатура от слов МЕТАболический ПРОТектор) — противоастени- ческий препарат с психоактивирующими и ноотропными свойствами. Длительное время использовался в восстановительной, спортивной и военной медицине. Действие этилтиобензимидазола реализуется через активацию синтеза РНК и белков в нервной и мышечной ткани, повышение микроциркуляции в важнейших органах и тканях (миокард, мозг, печень). Препарат оптимизирует энергопродукцию и энерготраты, в основном за счет более экономичного расходования АТФ и стимуляции глюконеогенеза, усиливает репаративные процессы в тканях.
Другим препаратом, оказывающим влияние на усталость, является близкий по структуре к амантадину Ладастен (Х-(2-адамантил)-Н-(парабромфенил)амин). Препарат обладает широким спектром терапевтического действия: способствует повышению физической и психической работоспособности, оказывает анксиолитический эффект. Ладастен малотоксичен при длительном применении, не вызывает привыкания, прекращение приема не сопровождается синдромом отмены. Это позволяет рекомендовать его для пробной терапии у пациентов с БП и усталостью. Эффективность Мета- прота и Ладастена не проверялась в плацебо-контроли- руемых исследованиях. К сожалению, на сегодняшний
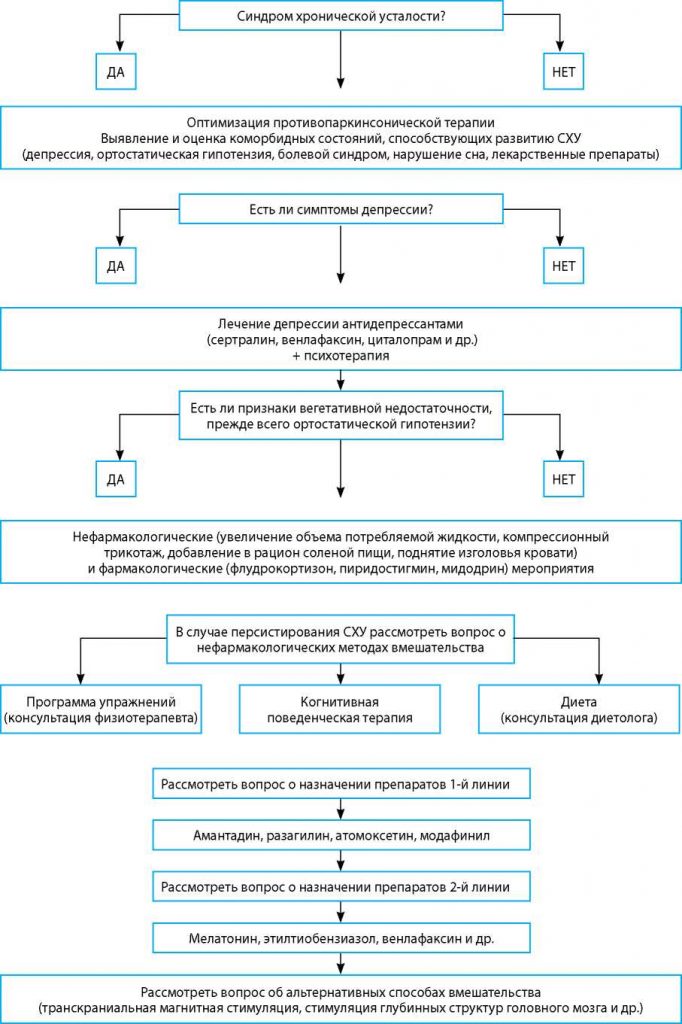
Рис. 2. Алгоритм коррекции синдрома хронической усталости при БП.
день исследования эффективности лечения СХУ при БП по продолжительности не превышали 8 нед. [39].
Алгоритм коррекции синдрома хронической усталости при БП представлен на рисунке 2.
[1] Центр экстрапирамидных заболеваний РМАНПО М3 РФ, кафедра неврологии.
Литература
- Аведисова А.С. Терапия астенических состояний // Фармацевтический вестник. — 2003. — №3 (282). — С. 15-16.
- Вознесенская Т.Г., Фокина НМ, Яхно Н.Н. Лечение астенических расстройств у пациентов с психовегетативным синдромом (результаты многоцентрового исследования эффективности и переносимости Ладастена®) // Жури, не- врол. и психиатр, им. С.С.Корсакова. — 2010. — №110 (5). — С. 17-26.
- Воробьева О.В. Многогранность феномена астении // РМЖ. — 2012. — №5. — С. 248-252.
- Воробьева О.В. Астенические состояния: эффективная и безопасная терапия // РМЖ. — 2009. — №20. — С. 1330— 1334.
- Кулуа Т.К, Федорова Н.В., Поповкина О.А. Ночные моторные симптомы болезни Паркинсона и их коррекция трехкомпонентным препаратом леводопа/карбидопа/энтакапон // Журн. неврол. и психиатр, им. С.С.Корсакова. — 2011. — С. 9.
- Левин О.С. Современные подходы к диагностике и лечению флуктуаций при болезни Паркинсона // Журн. неврол. и психиатр, им. С.С.Корсакова. — 2006. — №12. — С. 74-80.
- Левин О.С., Смоленцева П.Г. Немоторные проявления болезни Паркинсона. — М., 2007. — С. 19.
- Левин О.С., Смоленцева II.Г., Иванов А.К. Недвигательные флюктуации при болезни Паркинсона // Журн. неврол. и психиатр, им. С.С.Корсакова. — 2010. — №3. — С. 90-96.
- Левин О.С., Смоленцева П.Г., Цередсодном Б. Влияние дофаминергической терапии на нейропсихологические функции у больных болезнью Паркинсона // Неврол. журн. — 2004′- №3. — С. 31-37.
- Левин О.С., Нестерова О.С., Отческая О.В. Влияние агониста дофаминовых рецепторов прамипексола (мирапекс) на дрожательный гиперкинез, аффективные и когнитивные нарушения у пациентов с болезнью Паркинсона // Журн. неврол. и психиатр, им. С.С.Корсакова. — 2009. — Т. 109, №8.-С. 36^11.
- ЛевинО.С., ФедороваН.В. Болезнь Паркинсона.-М., 2012.
- Левин О.С., Датиева В.К. Новое в диагностике и лечении болезни Паркинсона: анализ результатов XIX Всемирного конгресса по болезни Паркинсона и смежным расстройствам (Шанхай, Китай). Бюллетень Национального общества по изучению болезни Паркинсона и расстройств движений. -2012. — С. 1-5.
- Нобель XI.P. Утомляемость при болезни Паркинсона // Журн. неврол. и психиатр, им. С.С.Корсакова. — 2009. — №9.-С. 23-26.
- Шток В.Н., Иванова-Смоленская НА., Левин О.С. Экс- трапирамидные расстройства. — М.: МЕДпресс-информ, 2002.-606 с.
- Alves G., Wentzel-Larsen Т, Larsen J.P. Is fatigue an independent and persistent symptom in patients with Parkinson’s disease? // — 2004. — Vol. 63. — P. 1908-1911.
- Barone P, Scarzella L., Antonini A. et al. Pramipexole versus sertraline in the treatment of depression in Parkinson’s disease // J Neurol. — 2005. — Vol. 4. — P. 1-7.
- G., DittnerA., FindleyL. etal. The Parkinson’s fatigue scale//ParkRelat Disord. -2005. — Vol. 11. -P. 49-55.
- Chaudhuri K.R., Schapira A.H.V. Non-motor symptoms of Parkinson’s disease: dopaminergic pathophysiology and treatment // Lancet Neurol. — 2009. — Vol. 8. — P. 464M74.
- Chaudhuri K.R., Healy D.G., Schapira A.H.V. Non-motor symptoms of Parkinson’s disease: diagnosis and management // Lancet Neurol. — 2006. — Vol. 5. — P. 235-245.
- Chou K.L., Persad C.C., Patil P.G. Change in fatigue after bilateral subthalamic nucleus deep brain stimulation for Parkinson’s disease // Parkinsonism and Related Disorders. — 2012. — Vol. 18.-P. 510-513.
- , LanX., Roche I. etal. Caffeine protects against MPTP- induced bloodbrain barrier dysfunction in mouse striatum // J Neurochem. -2008. — Vol. 107. -P. 1147-1157.
- Critchley P.H., XIalcolm G.P. Fatigue and melatonin in Parkinson’s Disease Neurol Neurosurg Psychiatry. — 1991. — Vol. 54. — P. 91-92.
- Friedman J.H., Friedman H. Fatigue in Parkinson’s disease: a nine-year follow-up // Mov Disord. — 2001. — Vol. 16. — P. 1120-1’122.
- Friedman J.H., Brown R.G. Fatigue in Parkinson’s Disease: A Review // Movement Disorders. — 2007. — Vol. 22, №3. — P. 297-308.
- Friedman J., Alves G. Fatigue Rating Scales Critique and Recommendations by the Movement Disorders Society Task Force on Rating Scales for Parkinson’s Disease // Mov Disord. — 2010. — Vol. 25, №7. — P. 805-822.
- Ghosh A., Roy A., MatrasJ. et al. Simvastatin inhibits the activation of p21ras and prevents the loss of dopaminergic neurons in a mouse model of Parkinson’s disease // — 2009. — Vol. 29.-P. 13543-13556.
- Goldstein D. Dysautonomia in Parkinson’s disease: neurocar- diological abnormalities // Lancet Neurol. — 2003. — Vol. 2. — P. 669-676.
- Hagell P, Brundin L. Towards an understanding of fatigue in Parkinson’s disease // J Neurol Neurosurg Psychiatry. — 2009. — Vol. 80. -P. 489—192.
- Jasinska-XIyga B., Heckman MG. Loss of ability to work and ability to live independently in Parkinson’s disease // Parkinsonism and Related Disorders. -2012. — Vol. 18. -P. 130-135.
- Lou J.S., Kearns G., Oken B. et al. Exacerbated physical fatigue and mental fatigue in Parkinson’s disease // Mov Disord. — 2001.-Vol. 16.-P. 190-196.
- Xlendonca D.A., Menezes K, Jog M.S. Methylphenidate improves fatigue scores in Parkinson’s disease: a randomized controlled trial // Mov Disord. — 2007. — Vol. 22. — P. 2070-2076.
- Xlenza XL, Dobkin R. Sleep Disturbances in Parkinson’s Disease//Mov Disord. -2010. -Vol. 25 (Suppl. 1). -S117-S122.
- , Xliwa T. Fatigue in Patients with Parkinson’s Disease: Impact on Quality of Life // Intern Med. — 2011. — Vol. 50. — P. 1553-1558.
- Xlorlev J. Undemutrition in older adults // Family Practice. — 2012.’-Vol. 29. — i89—i93.
- Nakamura T, Hirayama XI, Hara T. et al. Does cardiovascular autonomic dysfunction contribute to fatigue in Parkinson’s disease? // Mov Disord. — 2011. — Vol. 3.
- Pavese N, Xletta I’, Bose S.K. et al. Fatigue in Parkinson’s disease is linked to striatal and limbic serotonergic dysfunction // -2010.-Vol. 133.-P. 3434-3443.
- Perez-Lloret S., Rev XI. Factors related to orthostatic hypotension in Parkinson’s disease // Parkinsonism and Related Disorders.-2012.-Vol. 18.-P. 501-505.
- Schifitto G., Friedman J.H., OakesD. etal. Fatigue in levodopanaive subjects with Parkinson’s disease // — 2008. — Vol. 71,- P. 481—185.
- Seppi K, Weintraub D., Coelho XI. The Movement Disorder Society Evidence-Based Medicine Review Update: Treatments for the Non-Motor Symptoms of Parkinson’s Disease // Mov Disord. -2011. — Vol.’26, №3. — S42-S80.
- Falko P.O., Waldvogel D., Weller XL Fatigue and excessive daytime sleepiness in idiopathic Parkinson’s disease differently correlate with motor symptoms, depression and dopaminergic treatment 11 Eur J Neurol. -2010. — Vol. 17. -P. 1428-1436.
- van Hilt enJ. J., WeggemanXL, van der Velde E.A. Sleep, excessive daytime sleepiness and fatigue in Parkinson’s disease // J Neural Transm Park Dis Dement Sect. — 1993. — №5 (3). — P. 235-244.